納米酶智能篩選新紀元 大數據驅動藥物材料研發邁入臨床前測試
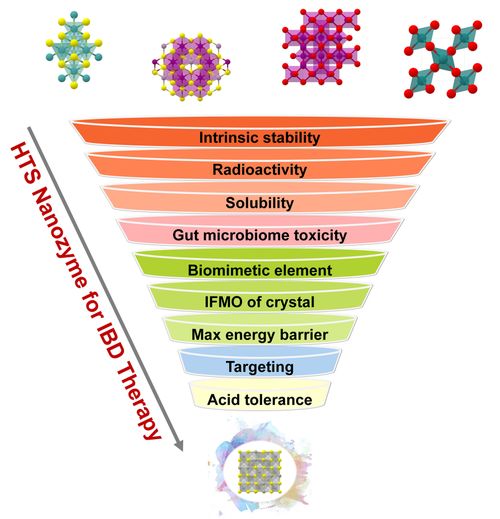
在當今藥物研發與材料科學交叉的前沿領域,一項突破性的進展正悄然改變著游戲規則。科學家們成功研發出一種創新的納米酶篩選策略,巧妙地將大數據技術與納米材料研發深度融合,為高效、精準的藥物與材料篩選開辟了新路徑。目前,該策略支撐的候選材料已順利進入臨床前測試階段,標志著從實驗室發現到實際應用的關鍵一步。
納米酶,即具有類酶催化活性的納米材料,因其穩定性高、成本相對較低且催化性能可調,在疾病診斷、治療(如腫瘤催化治療、抗菌)以及環境修復等領域展現出巨大潛力。傳統篩選方法依賴于試錯和有限的經驗,效率低下且難以系統探索龐大的材料化學空間。如何從數以萬計可能的成分、尺寸、形貌和表面修飾組合中,快速鎖定高性能納米酶,一直是制約其發展的瓶頸。
新研發的篩選策略核心在于構建一個集成化的智能平臺。研究團隊通過高通量實驗和文獻挖掘,建立了涵蓋多種納米材料(如金屬、金屬氧化物、碳基材料等)組成、結構參數與其催化活性(如氧化酶、過氧化物酶、超氧化物歧化酶等活性)之間關系的大型數據庫。利用機器學習算法,特別是深度學習模型,對這些多維、復雜的大數據進行訓練和分析。模型能夠學習并推斷出影響納米酶活性的關鍵物理化學描述符與微觀結構特征之間的隱藏規律,甚至預測尚未合成的新型納米材料的潛在酶活性。
這一數據驅動的策略實現了從“大海撈針”到“按圖索驥”的轉變。科學家可以輸入目標催化反應和所需的性能指標(如活性、選擇性、穩定性),由模型反向推薦最有可能實現該功能的納米材料組成與合成方案。這極大地加速了候選材料的發現與優化周期。例如,針對特定的腫瘤微環境,策略可以快速篩選出在弱酸性條件下具有高效過氧化物酶活性、能催化過氧化氫產生大量殺傷性羥基自由基的納米酶,用于腫瘤的催化治療。
基于該策略篩選出的明星納米酶材料,已在實驗室層面表現出卓越的性能。目前,針對某些特定適應癥(如某些實體瘤或耐藥菌感染)的納米酶制劑,已經啟動了系統的臨床前測試。這包括嚴格的體外細胞毒性、藥效學評估,以及動物模型體內的安全性、藥代動力學和療效研究。這些測試旨在驗證其治療潛力、生物相容性以及確定初步的給藥方案,為后續可能的臨床試驗奠定堅實基礎。
此項融合了納米技術、酶學與人工智能的篩選策略,其意義遠超單一材料的成功。它代表了一種研發范式的轉變:將材料研發從經驗導向轉變為數據與模型驅動的精準設計。隨著數據庫的不斷擴充和算法的持續優化,未來有望實現更廣泛功能性納米材料(不僅是納米酶,還包括藥物遞送載體、成像探針等)的理性設計與高效篩選。
通向臨床的道路依然需要跨越生物安全性、大規模生產穩定性、體內代謝機制明確化等多重關卡。但無疑,大數據賦能下的納米酶智能篩選策略,已經為下一代智能藥物與先進材料的研發引擎點燃了關鍵的火花,預示著個性化、高效能納米醫學解決方案的到來正加速成為現實。
如若轉載,請注明出處:http://www.phvirr.com.cn/product/60.html
更新時間:2026-01-06 13:22:54